I tuoi occhi

Malattie oculari
Glaucoma
Cos’è?
Il glaucoma è una patologia oculare cronica che evolve lentamente ma in modo irreversibile, spesso senza dare segnali evidenti nelle prime fasi. La malattia provoca un danno alle cellule nervose della retina e alla testa del nervo ottico (con conseguente compromissione del campo visivo) ed è spesso correlata a una pressione intraoculare elevata. Nel glaucoma, considerata ormai una patologia neurodegenerativa a tutti gli effetti, si verifica la morte di una specifica popolazione di cellule della retina, le cellule ganglionari. In un occhio sano, le cellule ganglionari svolgono un ruolo fondamentale: ricevono le informazioni luminose dai fotorecettori — che catturano le immagini — e le trasmettono al cervello attraverso gli assoni, che insieme formano il nervo ottico. Nel glaucoma, queste cellule vanno incontro a morte progressiva, interrompendo la comunicazione tra occhio e cervello e compromettendo così la vista. I danni provocati dal glaucoma possono sfociare in ipovisione o disabilità visiva, ma la buona notizia è che, se la malattia viene scoperta e trattata in tempo, è possibile fermarne la progressione. Per questo è fondamentale sottoporsi a controlli regolari e non trascurare eventuali segnali di alterazioni della vista: il glaucoma può essere silenzioso, ma una diagnosi precoce può davvero fare la differenza.
Epidemiologia
Il glaucoma rappresenta una delle principali cause di cecità nel mondo. Si stima che, nelle persone tra i 40 e gli 80 anni, la prevalenza del glaucoma ad angolo aperto sia intorno al 3,5%, mentre il glaucoma ad angolo chiuso colpisca circa lo 0,5% della popolazione. Secondo l’Organizzazione Mondiale della Sanità, nel mondo ci sono oltre 76 milioni di persone affette da questa malattia [1] e si prevede che il numero continuerà a crescere nei prossimi decenni a causa dell’invecchiamento della popolazione. Si tratta della seconda causa di cecità a livello planetario dopo la cataratta, ma è la prima a carattere irreversibile [2]. In Italia si stima che la malattia colpisca circa un milione di persone, ma quasi la metà non ne sarebbe a conoscenza perché non si sottopone regolarmente a controlli oculistici completi e a esami specifici come il fondo oculare, la tonometria e il campo visivo. Anche l’etnia gioca un ruolo nella prevalenza della patologia: il glaucoma ad angolo aperto è più diffuso nei soggetti di etnia nera, mentre il glaucoma ad angolo chiuso è più frequente nelle popolazioni dell’Asia orientale.
Fattori di rischio
- Pressione intraoculare: rappresenta il fattore di rischio più importante per lo sviluppo e la progressione del glaucoma, nonché l’unico bersaglio per le terapie attualmente a disposizione. La misurazione della pressione intraoculare rappresenta un cardine della valutazione iniziale e del follow-up dei pazienti con glaucoma o a rischio di svilupparlo (vedi “diagnosi”). Avere un alto valore di pressione intraoculare non significa avere il glaucoma. Sebbene sia diffusa l’idea che la malattia sia sempre legata a un aumento della pressione, molti pazienti con pressione considerata elevata (> 21 mmHg) non sviluppano necessariamente la malattia, mentre soggetti con pressione considerata “normale” possono sviluppare il cosiddetto “glaucoma a bassa pressione”.
- Età: rappresenta un fattore di rischio sia per lo sviluppo che per la progressione della malattia. Il glaucoma è raro prima dei 40 anni e si riscontra generalmente in individui di età più avanzata. Secondo alcune stime il glaucoma colpisce il 3,54% delle persone di età compresa tra i 40 e gli 80 anni [3]. La prevalenza della malattia cresce quindi significativamente all’aumentare dell’età della popolazione considerata.
- Etnia: i soggetti di etnia afro-americana mostrano un’incidenza maggiore di glaucoma primario ad angolo aperto, mentre le popolazioni asiatiche mostrano una maggiore incidenza di glaucoma da chiusura d’angolo.
- Familiarità: i parenti di primo grado di soggetti affetti da glaucoma sono più a rischio di svilupparlo rispetto alla popolazione generale.
- Miopia moderata/elevata
- Diabete
- Ipertensione e ipotensione sistemica
- Spessore corneale ridotto (non rappresenta un fattore di rischio indipendente per lo sviluppo o la progressione del glaucoma).
Altri fattori di rischio per lo sviluppo di glaucoma primario da chiusura d’angolo sono: l’età avanzata, la familiarità, il sesso femminile e l’ipermetropia.
COME SI PRODUCE L’AUMENTO DELLA PRESSIONE OCULARE?
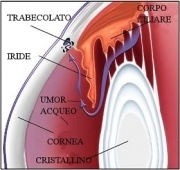
All’interno dell’occhio è presente un liquido chiamato umore acqueo, che viene continuamente prodotto e riassorbito. In questo senso, l’occhio può essere paragonato a un piccolo serbatoio con un rubinetto e una via di deflusso sempre aperti. Quando il deflusso dell’umore acqueo è ostruito, la pressione all’interno dell’occhio aumenta, determinando un rialzo della pressione intraoculare. Se questo aumento persiste nel tempo, il bulbo oculare può subire danni, in particolare a livello della testa del nervo ottico — la cosiddetta papilla ottica, situata nella parte centrale della retina. Poiché i danni al nervo ottico sono irreversibili, è fondamentale intervenire precocemente con una terapia adeguata.
COME SI PRODUCE IL DANNO ALLA VISTA?
La percezione visiva non riguarda soltanto l’oggetto che fissiamo, ma tutto ciò che lo circonda; l’insieme di ciò che riusciamo a vedere in un dato momento costituisce il cosiddetto campo visivo. Le immagini catturate dagli occhi vengono trasmesse dalla retina al cervello tramite il nervo ottico, che può essere paragonato a un cavo elettrico composto da milioni di fili, ciascuno dei quali trasporta informazioni relative a una piccola porzione del campo visivo. Il cervello, ricevendo questi segnali bioelettrici, riesce a ricostruire l’immagine nella sua interezza, permettendoci di percepire il mondo intorno a noi in modo coerente. Tuttavia, un aumento della pressione oculare può danneggiare irreparabilmente i neuroni responsabili di questo trasferimento di informazioni, come se i fili del “cavo” si logorassero. In particolare, la morte delle cellule ganglionari retiniche interrompe la comunicazione tra i fotorecettori della retina e il cervello, provocando una perdita di campo visivo. La gravità di questa perdita dipende dall’entità del danno: più cellule vengono compromesse, più importante sarà la riduzione della nostra capacità visiva. Pertanto, la salute delle cellule ganglionari, risulta fondamentale per mantenere una visione completa e nitida del mondo circostante. Esiste infatti una corrispondenza topografica per cui la perdita di cellule ganglionari in una specifica area della retina corrisponde alla perdita di una parte di campo visivo. Nel glaucoma, il danno inizia generalmente dalle fibre che trasportano le informazioni provenienti dalla periferia del campo visivo. In questa fase, la persona continua a vedere chiaramente l’oggetto su cui fissa lo sguardo, ma non si accorge che la visione laterale si sta progressivamente riducendo. Con l’avanzare della malattia, anche le fibre provenienti dalla macula, la zona centrale della retina responsabile della visione dettagliata, vengono danneggiate. Questo comporta una significativa riduzione dell’acuità visiva. Come avviene in molte patologie neurodegenerative, il danno causato dal glaucoma non è reversibile: se la malattia non viene trattata tempestivamente e con successo, può portare a una perdita della vista parziale o addirittura totale.
SINTOMI DELLA PRESSIONE OCULARE ALTA
Nelle varie forme di glaucoma, ad eccezione di quello acuto, la malattia insorge e si sviluppa senza che il paziente avverta sintomi particolari. Quando il soggetto si rende conto di non vedere bene nella parte periferica del proprio campo visivo, purtroppo i danni a carico delle fibre del nervo ottico sono già presenti. La visione centrale di solito è ben conservata, il visus può essere anche pari a 10/10, ma il paziente ha evidenti difficoltà nello svolgimento di azioni che sfruttano la parte periferica del campo visivo (scendere le scale, guidare, attraversare la strada).
I sintomi che possono comunque presentarsi in caso di pressione oculare alta sono:
- dolore agli occhi (localizzato in particolare sul sopracciglio);
- occhi arrossati;
- mal di testa;
- vista offuscata;
- aloni intorno alle luci;
- nausea;
- vomito;
- midriasi;
- fotofobia;
- lacrimazione.
Quali tipi di glaucoma esistono?
Con il termine glaucoma si indica un gruppo di patologie a diversa eziologia e con decorso clinico eterogeneo. A scopo meramente classificativo, si possono distinguere i glaucomi in due grandi famiglie: i glaucomi ad angolo aperto e i glaucomi da chiusura d’angolo, i quali differiscono significativamente per meccanismo patogenetico e per decorso clinico.
Ø Glaucoma primario ad angolo aperto (POAG)
Rappresenta la forma più comune di glaucoma nei paesi occidentali, è caratterizzata da un angolo irido-corneale di ampiezza normale. I principali fattori di rischio sono rappresentati da una pressione intraoculare (IOP) elevata e dall’età avanzata. La patogenesi del danno da POAG è, ad oggi, ancora incerta: si ritiene che la pressione intraoculare elevata, in concomitanza ad alterazioni vascolari, abbia un ruolo nell’induzione della morte delle cellule ganglionari retiniche e dei loro assoni, probabilmente ostacolando il normale trasporto assonale che avviene in queste cellule. L’aumento progressivo della pressione intraoculare sembra essere invece determinato da un aumento della resistenza a livello del trabecolato, ossia la parte dell’occhio deputata al filtraggio e allo “scarico” dell’umor acqueo: l’alterazione del trabecolato (dovuta all’età, allo stress ossidativo o ad altri fattori sconosciuti) comporta quindi una maggior difficoltà a drenare il liquido presente nell’occhio con conseguente incremento della pressione oculare . Una distinzione piuttosto arbitraria è stata proposta per dividere i POAG in base al livello di pressione intraoculare, esistono infatti i cosiddetti POAG a pressione elevata e i POAG a pressione normale: nel caso di questi ultimi i pazienti presentano livelli di pressione intraoculare considerati “normali” (di solito < 20 mmHg), oltre ad avere delle caratteristiche cliniche peculiari. Si ritiene che nel caso dei POAG a pressione normale, fattori di rischio diversi dalla pressione intraoculare elevata abbiano un particolare peso specifico nel determinare l’inizio e il peggioramento della malattia; tuttavia i principi di trattamento rimangono gli stessi (vedi sezione “terapia”).
· ØPOAG sospetto ed ipertensione oculare
Può sembrare paradossale, ma non sempre le visite e gli esami strumentali riescono a fornire una chiara indicazione sul fatto che il paziente possa essere sano o affetto da glaucoma. Una percentuale non trascurabile di pazienti infatti, soprattutto in fase iniziale di malattia, vengono considerati con sospetto glaucoma. Questi soggetti presentano uno o più segni clinici suggestivi per glaucoma, ad esempio un aspetto della papilla ottica o un esame del campo visivo più o meno alterati, una pressione oculare borderline, misurazioni OCT che deviano dai valori normali; ma nessuno di questi esami è alterato in modo significativo o comunque in maniera concorde rispetto agli altri. Soltanto il tempo e la ripetizione periodica dei suddetti esami di solito riescono a chiarire il quadro clinico del paziente. Sarà l’oculista a stabilire se, nel frattempo, il paziente dovrà eseguire una terapia o meno, in base ai dati a disposizione e ai fattori di rischio di ciascun individuo. Soggetti con pressione oculare superiore ai valori considerati normali (> 21 mmHg) ma con nervo ottico sano, campo visivo normale, anatomia non suggestiva di possibile chiusura angolare e nessun altro fattore di rischio per glaucoma, sono definiti ipertesi oculari. Avere una pressione oculare elevata NON significa avere il glaucoma. Anche in questo caso, sarà l’oculista a valutare la necessità di una terapia e a programmare gli esami di follow-up, in base al rischio di conversione da ipertensione oculare a glaucoma.
Ø Glaucomi secondari ad angolo aperto
Costituiscono un gruppo di patologie accomunate dal riscontro di un angolo irido-corneale aperto, dallo sviluppo di un danno al nervo ottico di tipo glaucomatoso e, cosa che le differenzia dai glaucomi primari, da una causa chiaramente responsabile dello sviluppo della malattia. Di seguito, verranno brevemente trattati soltanto i glaucomi secondari più frequenti.
- Glaucoma Pseudoesfoliativo
È il più frequente, ed è associato alla Sindrome Pseudoesfoliativa (detta anche PEX). È una situazione clinica caratterizzata dalla produzione di materiale furfuraceo da parte della superficie del cristallino che esfoliandosi intasa le vie di deflusso dell’umore acqueo (trabecolato) depositandosi a livello dell’angolo irido-corneale. Pertanto, nel tempo si determina un aumento della pressione intraoculare (IOP) e, di conseguenza, un glaucoma. Inoltre il materiale furfuraceo può depositarsi a livello dell’apparato di sospensione del cristallino al corpo ciliare (fibre zonulari), creando un indebolimento di tali fibre e una dislocazione del cristallino (sublussazione).Con il termine glaucoma si indica un gruppo di patologie a diversa eziologia e con decorso clinico eterogeneo. A scopo meramente classificativo, si possono distinguere i glaucomi in due grandi famiglie: i glaucomi ad angolo aperto e i glaucomi da chiusura d’angolo, i quali differiscono significativamente per meccanismo patogenetico e per decorso clinico
Ø Glaucoma primario ad angolo aperto (POAG)
Rappresenta la forma più comune di glaucoma nei paesi occidentali, è caratterizzata da un angolo irido-corneale di ampiezza normale. I principali fattori di rischio sono rappresentati da una pressione intraoculare (IOP) elevata e dall’età avanzata. La patogenesi del danno da POAG è, ad oggi, ancora incerta: si ritiene che la pressione intraoculare elevata, in concomitanza ad alterazioni vascolari, abbia un ruolo nell’induzione della morte delle cellule ganglionari retiniche e dei loro assoni, probabilmente ostacolando il normale trasporto assonale che avviene in queste cellule. L’aumento progressivo della pressione intraoculare sembra essere invece determinato da un aumento della resistenza a livello del trabecolato, ossia la parte dell’occhio deputata al filtraggio e allo “scarico” dell’umor acqueo: l’alterazione del trabecolato (dovuta all’età, allo stress ossidativo o ad altri fattori sconosciuti) comporta quindi una maggior difficoltà a drenare il liquido presente nell’occhio con conseguente incremento della pressione oculare . Una distinzione piuttosto arbitraria è stata proposta per dividere i POAG in base al livello di pressione intraoculare, esistono infatti i cosiddetti POAG a pressione elevata e i POAG a pressione normale: nel caso di questi ultimi i pazienti presentano livelli di pressione intraoculare considerati “normali” (di solito < 20 mmHg), oltre ad avere delle caratteristiche cliniche peculiari. Si ritiene che nel caso dei POAG a pressione normale, fattori di rischio diversi dalla pressione intraoculare elevata abbiano un particolare peso specifico nel determinare l’inizio e il peggioramento della malattia; tuttavia i principi di trattamento rimangono gli stessi (vedi sezione “terapia”).
- POAG sospetto ed ipertensione oculare
- Glaucomi secondari ad angolo aperto
Come si presenta la PEX?
Può essere evidenziata dall’oculista durante l’esame obiettivo con la lampada a fessura (meglio ancora se con la pupilla dilatata). Si potrà ben vedere il deposito del materiale furfuraceo sulla faccia anteriore del cristallino, distribuito in maniera circolare in campo pupillare e in periferia, assente laddove l’iride compie un movimento di sfregamento.
Quali sono gli aspetti caratteristici del glaucoma pseudoesfoliativo?
Di solito colpisce entrambi gli occhi (ossia è bilaterale) e spesso le alterazioni riscontrate sono asimmetriche nei due occhi; si evidenziano valori della pressione oculare piuttosto elevati, che possono subire importanti fluttuazioni nell’ambito delle 24 ore; ha un’evoluzione abbastanza rapida; c’è maggiore predisposizione allo sviluppo della cataratta; è presente una maggiore percentuale di complicanze durante e dopo gli interventi di cataratta; la pupilla si dilata con più difficoltà.
Come si cura il glaucoma pseudoesfoliativo?
Il trattamento di prima scelta è quello di tipo farmacologico, con l’instillazione di colliri che servono ad abbassare la pressione oculare (ipotonizzanti). La terapia deve essere tempestiva ed efficace per cui, se non si ottengono buoni risultati, all’inizio è bene ricorrere a più somministrazioni quotidiane (eventualmente con farmaci diversi). Il trattamento laser (trabeculoplastica) riceve spesso una buona risposta anche se non duratura, nel qual caso occorre ricorrere all’approccio chirurgico tramite l’intervento di trabeculectomia. È bene eseguire la facoemulsificazione quando è presente la cataratta (anche se in fase iniziale) e spesso anche quando il cristallino è ancora trasparente. Tale intervento, infatti, può indurre un significativo abbassamento della pressione intraoculare.
Inoltre, se effettuato precocemente è meno rischioso, in quanto la pupilla ha ancora una buona capacità dilatativa, c’è un basso rischio di dislocazione del cristallino nel vitreo durante l’operazione e si semplifica, infine, l’eventuale intervento di trabeculectomia (più facile da eseguire se il cristallino è già stato asportato in precedenza). Vale la pena, infine, ricordare l’importanza di controlli regolari per chi avesse una sindrome pseudoesfoliativa, ma non presenta ancora glaucoma. La misurazione periodica del tono, con esecuzione del campo visivo e della pachimetria nei casi sospetti (pressione oculare lievemente oltre i limiti della norma), aiuta a fare una diagnosi precoce e, quindi, a iniziare la giusta terapia prima che compaiano gravi danni oculari.
- Glaucoma Pigmentario:
È associato alla sindrome da dispersione di pigmento. In questi pazienti, una particolare conformazione di alcune strutture intraoculari determina la liberazione di pigmento nell’umor acqueo, con conseguente alterazione della funzione trabecolare e incremento della pressione intraoculare. È più frequente nei maschi over 30. Alcune caratteristiche tipiche di questa condizione rendono generalmente agevole il riconoscimento di tale sindrome nei pazienti affetti da parte dell’oculista, che dovrà valutare la presenza o meno di glaucoma e la necessità o meno di una terapia. Le terapie e gli esami di follow-up sono gli stessi del POAG.
Altri glaucomi secondari ad angolo aperto:
- Glaucoma uveitico: associato ad uveiti infettive o non infettive;
- Glaucoma neovascolare: temibile conseguenza di patologie vascolari oculari o della retinopatia diabetica avanzata;
- Glaucoma indotto da alterazioni del cristallino (traumi o cataratte ipermature);
- Glaucoma post-traumatico;
- Glaucoma post-chirurgico;
- Glaucoma da farmaci (in particolare dopo terapie cortisoniche prolungate).
Ø Glaucomi da chiusura angolare
Eterogeneo gruppo di condizioni patologiche che condividono, come principale responsabile dell’incremento della pressione intraoculare, e successivamente del danno glaucomatoso, l’apposizione della periferia iridea al trabecolato, la cosiddetta chiusura angolare. In questa condizione, il deflusso dell’umor acqueo attraverso il trabecolato viene ostacolato meccanicamente e si possono verificare quadri clinici più o meno severi ed eclatanti, dal glaucoma acuto alla chiusura angolare intermittente. I meccanismi patogenetici con i quali si innesca la chiusura angolare sono molteplici, il più frequente è il cosiddetto blocco pupillare (circa 2/3 dei casi), ossia il blocco del passaggio dell’umor acqueo attraverso il forame pupillare; altri meccanismi di induzione della chiusura angolare sono riconducibili ad alterazioni dell’anatomia dell’iride (iris plateau), ad alterazioni a livello del cristallino, ad alterazioni nella porzione posteriore dell’occhio, a somministrazione di farmaci o interventi di chirurgia oculare. I glaucomi da chiusura d’angolo sono meno frequenti nel mondo occidentale (vedi fattori di rischio), ma abbastanza frequenti per costituire una minaccia non trascurabile soprattutto in pazienti con determinati fattori di rischio, come l’ipermetropia. Il rischio di glaucoma da chiusura d’angolo deve essere sempre valutato dall’oculista durante le visite oculistiche di follow-up, perché in presenza di condizioni predisponenti, l’esecuzione di determinate procedure laser o chirurgiche (rispettivamente l’iridotomia YAG laser e l’intervento di cataratta a scopo idrodinamico) possono abbattere o addirittura eliminare l’eventualità futura di una chiusura angolare.
- Chiusura angolare acuta: evento clinico drammatico, caratterizzato da valori molto elevati di pressione intraoculare (> 50 mmHg), sintomatologia tipica (dolore oculare acuto e intenso, cefalea frontale, riduzione dell’acuità visiva, nausea e vomito) e chiari segni riscontrabili all’esame dell’occhio (pupilla in media midriasi, edema corneale, camera anteriore periferica di profondità molto ridotta, iniezione pericheratica). Rappresenta una vera e propria emergenza oculistica e, se non trattata prontamente, può comportare un danno irreversibile della funzione visiva dell’occhio colpito. La terapia consiste in una combinazione di farmaci topici o sistemici per ridurre la pressione oculare e nell’esecuzione di una iridotomia YAG laser o di pratiche chirurgiche più o meno invasive per eliminare il meccanismo di innesco della chiusura angolare.
Ø Glaucoma congenito
In questa forma della patologia oculare il sistema di drenaggio è “cattivo” sin dalla nascita. Per questo motivo si verifica un aumento di pressione intraoculare. Il bambino presenta fastidio alla luce (fotofobia) e lacrimazione eccessiva. L’aumento pressorio può causare un aumento delle dimensioni dell’occhio (nei piccoli le pareti oculari sono meno resistenti) e la cornea può divenire opaca. Ogni sintomo sospetto deve indurre i genitori ad andare dall’oculista per effettuare una visita di controllo. Questo tipo di glaucoma è però raro: colpisce un neonato ogni diecimila.
Diagnosi
L’unico modo per individuare precocemente il glaucoma è sottoporsi regolarmente a una visita oculistica completa. Prima di iniziare l’esame vero e proprio, l’oculista raccoglie i dati anamnestici del paziente, cercando di comprendere eventuali disturbi già presenti e verificando se in famiglia ci siano casi di glaucoma, poiché l’ereditarietà rappresenta un fattore importante nello sviluppo della malattia. Di seguito verranno elencati i principali esami eseguiti nella diagnosi e nel follow-up dei pazienti con glaucoma o con sospetto glaucoma.
Visita oculistica
Permette di valutare le diverse strutture dell’occhio coinvolte nello sviluppo e nella progressione della malattia. Durante l’esame, l’oculista può verificare, tra le altre cose, l’ampiezza della camera anteriore, importante nel glaucoma ad angolo chiuso, individuare eventuali cause di glaucoma secondario come la sindrome pseudoesfoliativa, la sindrome da dispersione di pigmento o la neovascolarizzazione, e osservare l’aspetto della testa del nervo ottico per identificare l’eventuale presenza di un danno da glaucoma più o meno avanzato. La visita oculistica deve comprendere la valutazione del fondo dell’occhio, preferibilmente in midriasi (mediante dilatazione della pupilla). In base alla gravità della malattia, alla rapidità di progressione della stessa, al tempo trascorso dalla diagnosi e a numerosi altri fattori, l’oculista deciderà quando eseguire la visita e/o gli esami di follow-up, generalmente in un tempo compreso tra i 3 e i 12 mesi. È importante ricordare come il glaucoma sia una malattia cronica, da cui non si può guarire; è necessario dunque effettuare delle visite e degli esami per tutta la vita, in modo tale da accorgersi per tempo di eventuali peggioramenti della malattia e prendere le giuste contromisure terapeutiche.
Misurazione della pressione oculare
La tonometria, uno degli esami fondamentali durante la visita oculistica, è un elemento chiave nella valutazione dei pazienti con glaucoma e nel monitoraggio dell’efficacia della terapia ipotonizzante. Esistono diversi strumenti per misurare la pressione intraoculare, ma il riferimento standard è il tonometro ad applanazione di Goldmann. Questo esame non è né doloroso né invasivo: lo strumento sfiora delicatamente la superficie dell’occhio dopo l’applicazione di un collirio anestetico e di un colorante (fluoresceina), permettendo di ottenere una misurazione accurata della pressione oculare. Oltre al tonometro ad applanazione, esistono altri strumenti per misurare la pressione intraoculare, come il tonometro a soffio e quello a rimbalzo. Questi dispositivi non sono invasivi e possono essere utilizzati senza l’applicazione del collirio anestetico o del colorante. La misurazione della pressione oculare può essere effettuata una sola volta nell’arco della giornata oppure più volte, a seconda delle necessità cliniche e della valutazione dell’oculista, ad esempio per eseguire una curva tonometrica e monitorare meglio le variazioni della pressione durante il giorno.
Esame del campo visivo
Esame strumentale che non può mancare nell’inquadramento diagnostico e nel monitoraggio dei pazienti con glaucoma o con sospetto glaucoma. Il campo visivo è la porzione di spazio che può essere percepita da un occhio ed il danno causato dal glaucoma consiste nella riduzione progressiva dell’estensione del campo visivo stesso. Gli strumenti a nostra disposizione (detti perimetri), riescono a rilevare danni al campo visivo molto precocemente, prima che il paziente stesso sviluppi dei sintomi. L’esame non è invasivo e consiste nel proiettare degli stimoli luminosi sullo sfondo chiaro del perimetro, la percezione di tali stimoli da parte del paziente dovrà essere confermata premendo un pulsante. Eseguire un campo visivo in modo tale che sia attendibile richiede un certo grado di collaborazione e concentrazione da parte del paziente, possono quindi essere necessari diversi esami prima che il paziente acquisisca l’esperienza necessaria ad eseguirlo in maniera corretta. Così come la visita oculistica, anche il campo visivo deve essere ripetuto a intervalli regolari, a discrezione dell’oculista.
OCT
Acronimo di tomografia a coerenza ottica, l’OCT è un esame strumentale non invasivo, che consente di ottenere immagini tomografiche ad alta risoluzione delle strutture coinvolte nel danno glaucomatoso. L’OCT costituisce un importante ausilio per l’oculista nella valutazione della morfologia di tali strutture ed è complementare alla visita oculistica con esame del fondo dell’occhio. Gli strumenti attualmente a disposizione riescono a fornire delle immagini a risoluzione e dettaglio molto elevati. L’OCT ha ormai affiancato la visita oculistica e il campo visivo nella diagnosi e nel follow up dei pazienti con glaucoma conclamato o sospetto e la periodicità con cui ripetere l’esame è stabilita dall’oculista.
Pachimetria
È la misurazione dello spessore della cornea (la porzione più anteriore dell’occhio) con strumenti che richiedono o meno il contatto con la superficie dell’occhio. Viene generalmente eseguita una sola volta e dovrebbe far parte degli esami di inquadramento di tutti i pazienti glaucomatosi o con sospetto glaucoma. Avere una cornea sottile rappresenta un fattore di rischio non indipendente per lo sviluppo o la progressione del glaucoma, ma la pachimetria è strettamente correlata anche alla misurazione della pressione oculare: valori pachimetrici che deviano significativamente dai valori medi riscontrati nella popolazione generale possono infatti indurre delle sovrastime o delle sottostime della pressione intraoculare; in particolare, cornee spesse forniranno pressioni più alte del valore reale, cornee sottili forniranno pressioni più basse del valore reale.
Gonioscopia
Rappresenta l’esame diretto dell’angolo irido-corneale, ossia la regione della porzione anteriore dell’occhio (detta camera anteriore) dove l’iride e la cornea si incontrano. Questa regione anatomica è di fondamentale importanza per la fisiologia oculare in quanto è qui che risiedono le strutture deputate al drenaggio dell’umor acqueo, ossia il liquido che circola all’interno dell’occhio e la cui pressione idrostatica determina la pressione intraoculare . Nei glaucomi da chiusura d’angolo, questa regione anatomica risulta essere ridotta in ampiezza, tale da ostacolare il deflusso dell’umor acqueo e il mantenimento della pressione intraoculare fisiologica. L’esame necessita dell’applicazione di una lente apposita sulla superficie dell’occhio, previa instillazione di collirio anestetico, e di osservazione dell’angolo irido-corneale alla lampada a fessura. La gonioscopia dovrebbe essere eseguita almeno una volta in tutti i pazienti con diagnosi di glaucoma o con glaucoma sospetto, in particolare nei pazienti a rischio di glaucoma da chiusura d’angolo.
Terapia
Secondo le attuali linee guida, l’obiettivo della terapia del glaucoma non è semplicemente la riduzione della pressione oculare: il traguardo che ci si pone è quello di migliorare la qualità di vita del paziente glaucomatoso, o a rischio di glaucoma, a un costo sostenibile per la società. Per questo la decisione su quale terapia utilizzare e su quando iniziarla va personalizzata per ogni paziente. Questo perché non solo la malattia, ma anche la terapia stessa ha un impatto sulla qualità di vita del paziente, nonché sui costi per la società. Attualmente, il medico oculista non ha modo di guarire il danno glaucomatoso quando questo si è già reso manifesto. Può soltanto rallentare la progressione, e questo attualmente si può ottenere solo riducendo la pressione oculare fino a quel valore ideale, caratteristico per ogni paziente (IOP target), raggiunto il quale la riduzione delle cellule ganglionari retiniche diventa simile a quella che si ha fisiologicamente con l’avanzare dell’età. Le armi a disposizione per ridurre la progressione del danno da glaucoma sono la terapia medica, quella laser e quella chirurgica.
La terapia medica prevede l’instillazione quotidiana di farmaci in collirio. Le classi di farmaci utilizzate nella terapia del glaucoma sono gli analoghi delle prostaglandine, i beta bloccanti, gli inibitori dell’anidrasi carbonica, gli alfa-2 agonisti e i parasimpaticomimetici. È stata identificata anche una categoria più recente, gli inibitori delle rho chinasi. In casi selezionati, e generalmente nel breve termine, possono essere utilizzati anche farmaci con modalità di somministrazione diversa da quella in collirio, come il mannitolo, diuretico osmotico somministrato per via endovenosa, o l’acetazolamide in compresse. Ogni classe di farmaci ha uno specifico profilo per quanto concerne gli effetti collaterali e l’efficacia ipotonizzante: si va da una riduzione della pressione oculare da un minimo del 20% a un massimo del 35-40% per singolo principio attivo e possono essere utilizzate, da sole o in combinazione, fino al raggiungimento della IOP target. Affinché la terapia medica sia efficace è fondamentale che il medico oculista responsabilizzi il paziente e gliene spieghi l’importanza, nonché gli effetti collaterali che potrebbe aspettarsi; è altrettanto importante che il paziente sia in grado di autosomministrarsi il collirio, o farselo somministrare da terzi, con precisione e costanza. Tuttavia, se la terapia medica non è ben tollerata o non si dimostra sufficiente ad impedire la progressione della malattia, si pone indicazione alla chirurgia.
La terapia laser prevede la trabeculoplastica laser selettiva (SLT) e la trabeculoplastica argon laser (ALT). Entrambe non necessitano di ospedalizzazione, possono essere eseguite in ambulatorio e permettono una riduzione della pressione oculare media fino al 25%. Possono essere utilizzate come unica terapia, o in associazione a terapia medica o chirurgica. Non sono indicate nelle forme di glaucoma ad angolo chiuso, infiammatorie o neovascolari. Anche l’attacco acuto di glaucoma si giova della terapia laser: se presente un blocco pupillare, questo può essere risolto da un’iridotomia YAG laser, che permette di ristabilire la normale idrodinamica tra la camera posteriore e anteriore dell’occhio. La tecnica chirurgica tradizionale del glaucoma, nonché quella tuttora riconosciuta come gold standard, è la trabeculectomia. L’intervento prevede di creare una fistola tra la camera anteriore dell’occhio e lo spazio sotto la congiuntiva per permettere una via alternativa di deflusso dell’umore acqueo tramite una bozza filtrante. Altra possibilità è l’impianto di una valvola o di un tubo drenante, che solitamente vengono riservati ai casi più complessi, dove la chirurgia tradizionale ha fallito o rischia di fallire per la cicatrizzazione della bozza filtrante.
Altre tecniche possibili sono la sclerectomia profonda, la viscocanalostomia e la canaloplastica. Queste, se da una parte sono meno invasive rispetto alla trabeculectomia, dall’altra sembrerebbero avere una minore efficacia ipotonizzante e sono pertanto meno praticate.
Un’altra possibilità sono le cosiddette MIGS, acronimo per minimally invasive glaucoma surgeries. Queste prevedono l’utilizzo di diversi dispositivi che possono incentivare il deflusso dell’umor acqueo tramite vie diverse, bypassando il trabecolato per permettere all’acqueo di raggiungere il canale di Schlemm, dilatando il canale stesso, oppure oltrepassandolo direttamente per creare uno spazio di deflusso sottocongiuntivale. Queste tecniche prevedono una minore manipolazione chirurgica, un più rapido recupero postoperatorio e un tasso di complicanze piuttosto ridotto. Per contro, sembrano avere un’efficacia ipotonizzante minore rispetto all’intervento classico di trabeculectomia. Vengono di solito riservati a pazienti sui quali non è necessaria una drastica riduzione della pressione oculare. È importante comunque ricordare che la scelta del trattamento va attentamente calibrata per ogni paziente in base al quadro clinico e spetta sempre al chirurgo.
Da ricordare, infine, che anche la chirurgia della cataratta può contribuire enormemente alla riduzione della pressione oculare nelle chiusure angolari indotte dal cristallino.
La pressione intraoculare (Faq)
Da cosa è determinata la pressione degli occhi?
La pressione intraoculare (IOP) dipende principalmente dalla quantità di un liquido prodotto all’interno dell’occhio, chiamato umor acqueo. In pratica, più liquido è presente nel bulbo oculare, maggiore sarà la pressione.
Con quale unità si misura?
Il valore della pressione interna dell’occhio, sebbene differente dalla pressione arteriosa, viene misurato con la stessa unità: i millimetri di mercurio (mmHg). Tradizionalmente, l’oculistica considerava i due valori completamente indipendenti. Tuttavia, studi recenti hanno evidenziato l’esistenza di una certa correlazione: secondo alcuni ricercatori, chi ha una pressione arteriosa elevata potrebbe avere maggiori probabilità di sviluppare una pressione intraoculare alta, anche se la relazione rimane relativamente debole [5].
Qual è il valore massimo tollerabile dall’organismo? 
La pressione intraoculare dovrebbe normalmente essere compresa tra 10 e 20 millimetri di mercurio (mmHg). Il glaucoma è generalmente associato a valori superiori a 20-21 mmHg, ma esiste anche una forma a bassa pressione, in cui il nervo ottico subisce danni pur con valori pressori considerati normali. Questo tipo di glaucoma sembra legato a un ridotto afflusso di sangue al nervo ottico, che provoca una progressiva atrofizzazione delle fibre nervose. Inoltre, nella valutazione della pressione oculare è importante considerare lo spessore della cornea e l’eventuale presenza di una miopia elevata.
Come si misura la pressione intraoculare?
Esistono diversi metodi per misurare la pressione intraoculare, e nel corso degli anni le tecniche si sono evolute, raggiungendo maggiore precisione. Attualmente, negli ospedali, lo strumento più diffuso è il tonometro ad applanazione di Goldmann, che misura la resistenza del bulbo esercitando una leggera pressione sulla cornea. Per gli screening di massa, invece, si utilizza più comunemente il tonometro a soffio, che non richiede contatto diretto con l’occhio, ma sfrutta un getto d’aria indirizzato sulla cornea. (Vedi tonometria).
Quali possono essere altri esami utili?
Può essere utile misurare lo spessore della cornea mediante un esame strumentale chiamato pachimetria, per determinare il valore “reale” della pressione oculare. In particolare, nelle persone con una cornea sottile (pachimetria più bassa) è necessario aumentare di alcuni punti la pressione rilevata per ottenere una misurazione corretta (reale). Al contrario, negli individui con cornea più spessa (pachimetria più alta) bisogna sottrarre alcuni punti dalla rilevazione tonometrica.
Quando bisogna effettuare la pachimetria?
È sufficiente eseguire la pachimetria corneale una sola volta, dal momento che lo spessore della cornea non si modifica in maniera significativa nel tempo, a differenza di altri esami quali il campo visivo o l’OCT che devono essere invece ripetuti periodicamente per monitorare l’eventuale evoluzione del glaucoma.
Come si tratta il glaucoma?
Si cura di solito con colliri per abbassare la pressione oculare (detti “ipotonizzanti”). Per risultare efficace la terapia deve essere eseguita regolarmente e con costanza. In alcuni casi, la terapia può provocare effetti indesiderati: alcune gocce possono causare bruciore, arrossamento degli occhi o mal di testa, generalmente transitori e destinati a scomparire dopo poche settimane. Talvolta possono verificarsi anche piccole alterazioni del ritmo cardiaco, di solito di scarsa rilevanza. Chi dovesse accusare fastidi o disturbi deve sempre informare il proprio medico oculista.
Le persone affette da glaucoma necessitano di controlli periodici, poiché la malattia può peggiorare senza dare sintomi evidenti. In questi casi può essere necessario modificare la terapia. Una volta che il danno al nervo ottico si è verificato, non è più reversibile: si ricorre quindi a farmaci e, se necessario, alla chirurgia (come la trabeculectomia) per cercare di preservare la funzionalità visiva residua.
Il trattamento del glaucoma è efficace solo se la terapia prescritta dal medico oculista viene seguita scrupolosamente. In alcuni casi possono essere consigliati integratori alimentari che contribuiscono alla protezione del nervo ottico. La terapia non deve mai essere sospesa senza consultare l’oculista e il medico di famiglia dovrebbe sempre essere informato dei farmaci in uso. Se i colliri non riescono a controllare adeguatamente la pressione intraoculare, può rendersi necessario ricorrere alla chirurgia o al laser. Le complicanze di questi interventi sono rare, e nella maggior parte dei casi consentono di impedire la progressione della malattia, che altrimenti potrebbe portare a ipovisione o cecità.
Quand’è più probabile che una persona sia affetta da glaucoma?
Quando ha più di quarant’anni e ci sono altri casi in famiglia (per questo si parla di “familiarità” per il glaucoma). Più si è anziani e più aumenta il rischio di essere colpiti da questa patologia oculare detta anche “silente” perché non dà sintomi particolari nelle fasi iniziali. Soprattutto chi ha altri familiari con glaucoma dovrebbe sottoporsi indicativamente a un controllo oculistico una volta l’anno anche in assenza di altre patologie (con misurazione della pressione oculare). La maggiore incidenza di glaucoma sarebbe favorita anche dalla presenza di miopia o ipermetropia elevate, dal diabete e da eventuali terapie protratte a base di cortisonici.
[1] I dati sono stati pubblicati nel 2010. Più recentemente, nel 2017, il Vision Loss Expert Group ha citato la cifra di 60 milioni (AAVV, “Global causes of blindness and distance vision impairment 1990–2020: a systematic review and meta-analysis”, Lancet Glob Health. 2017 Dec;5(12):e1221-e1234. doi: 10.1016/S2214-109X(17)30393-5. Epub 2017 Oct
[2] Fonte: IAPB Internaz.
[3] Fonte: Tham YC, Li X, Wong TY, Quigley HA, Aung T, Cheng CY, “Global prevalence of glaucoma and projections of glaucoma burden through 2040: a systematic review and meta-analysis“, Ophthalmology. 2014 Nov;121(11):2081-90. doi: 10.1016/j.ophtha.2014.05.013. Epub 2014 Jun 26. Review.
[4] “Diffuse anomalie strutturali e funzionali nel cervello di un glaucomatoso possono essere, almeno parzialmente, indipendenti da una IOP più elevata (=pressione intraoculare, ndr) e dalla conseguente degenerazione retinica”, cit. tratta dall’articolo di Giorgio A, Zhang J, Costantino F, De Stefano N, Frezzotti P, “Diffuse brain damage in normal tension glaucoma“, Human Brain Mapping, 2017 Oct 24. doi: 10.1002/hbm.23862 (Epub ahead of print)
[5] Horwitz A, Klemp M, Jeppesen J, Tsai JC, Torp-Pedersen C, Kolko M, “Antihypertensive Medication Postpones the Onset of Glaucoma: Evidence From a Nationwide Study“,
Hypertension. 2017 Feb;69(2):202-210. doi: 10.1161/HYPERTENSIONAHA.116.08068. Epub 2016 Dec 5
Scheda informativa a cura dell’Agenzia internazionale per la prevenzione della cecità-IAPB Italia onlus.
Ultima revisione scientifica: 4 marzo 2026.
Leggi le condizioni generali di consultazione di questo sito.

Scrivi nel Forum: un medico oculista ti risponderà gratuitamente.
